“当时,本次论文的第一作者许仁珪同学在实验室休息间吃午饭,她用自热火锅加热包煮了一份火锅,我寻着香味来到休息间。突然我灵光一现,想起不久前和临床医生讨论过光热肿瘤治疗。于是我立刻和许仁珪研究加热包的工作原理,快速写下笔记并初步制定文献检索和实验尝试的计划。”华中科技大学基础医学院药理系教授陈伟表示。正是这个吃自热火锅的经历,让他们设计出一种水热响应多轮可触发微针(Hydrothermally responsive multi-round acturable microneedle , HRMAM)系统。
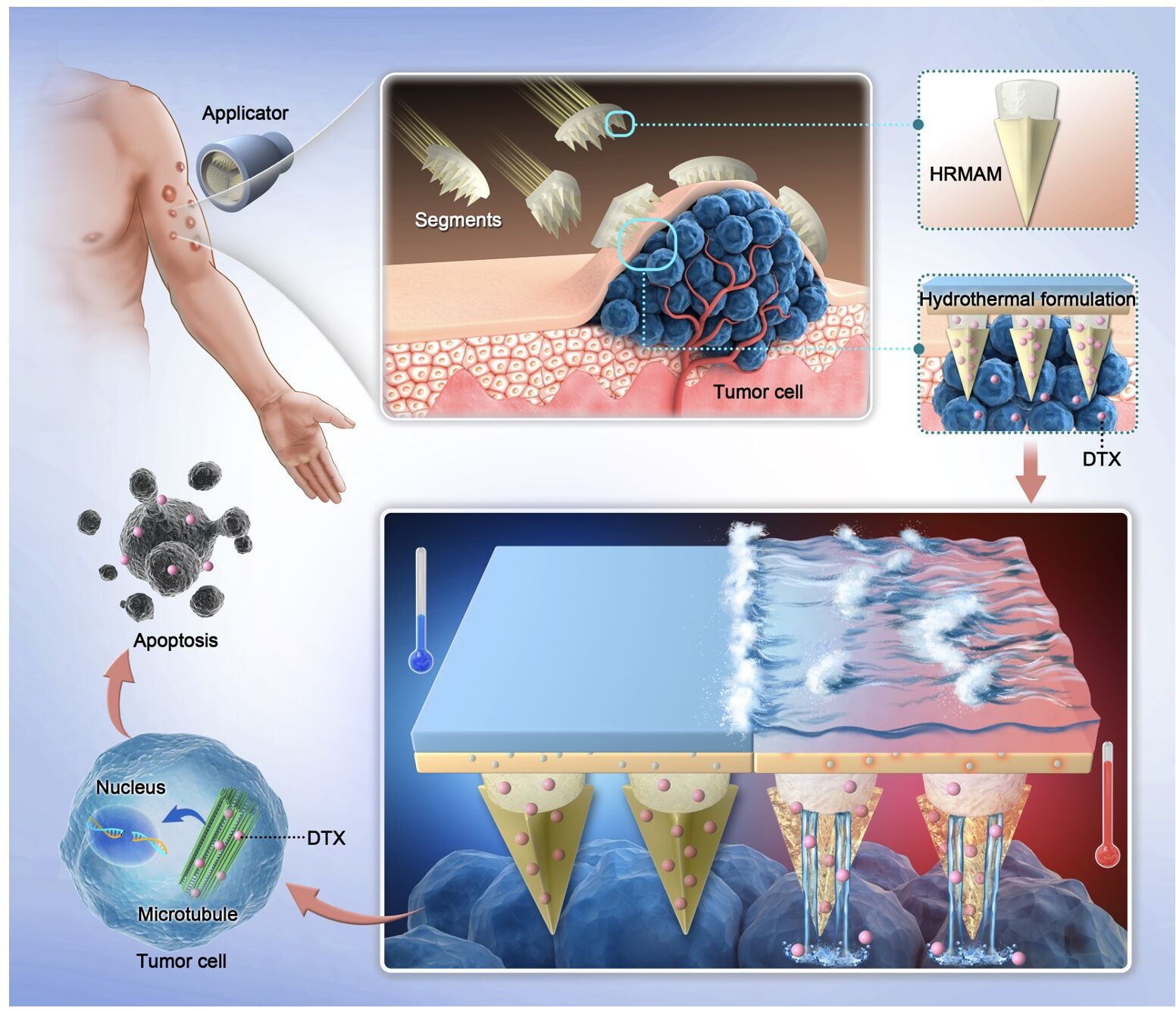
在难以触及的皮下肿瘤治疗过程中,凭借创伤小、操作方便、系统毒性低等优势,局部治疗展现出较大的潜力。临床上,光热治疗的原理在于利用光热转换材在肿瘤内的局部激活,进而诱导热力杀伤。这种疗法常被用于浅表皮肤癌、乳腺癌等肿瘤的治疗。然而,光热转换材的潜在毒性、对于特定复杂仪器的需求(近红外光源)、以及时空精准性的不足,制约着光热治疗的临床效果。
为了克服常规临床方案的不足,以及改善局部难以触及皮下肿瘤的痛点,课题组基于前期在生物医用器件领域的积累,以自热火锅水热系统和智能仿生刺形结构为启发,通过改良自热火锅加热包的配方,使其最高加热温度稳定在50-60°C,并将其整合于特殊设计的凹槽结构微针基底上,在少量液态水的作用之下,无需任何复杂设备即可触发水热反应,进而能够诱使微针基底形成热熔物。
在凹槽结构的介导下,基于毛细作用可以向深部组织渗透,从而递送临床药物多烯紫杉醇(Docetaxel, DTX)。此外,为了辅助HRMAM系统更好地贴合于不同形态的肿瘤,该团队还设计了一种凸面贴合施药器,三组扇形HRMAM贴片同时能嵌合于释药器之中,并能完美地附着于肿瘤表面。最终结果显示,在黑色素瘤和乳腺癌的动物模型中,HRMAM系统分别取得75.11%和72.29%的肿瘤生长抑制率,超越目前临床用药的局部直接递送效率,具备较高的临床转化潜力。未来,随着药物浓度和水热配方的进一步改善,治疗效果有望继续得到提升。另外,此次使用的微针材料主要是聚己内酯(PCL,Polycaprolactone),这是已被美国食品药品监督管理局(FDA,Food and Drug Administration)审批通过的生物医用材料。
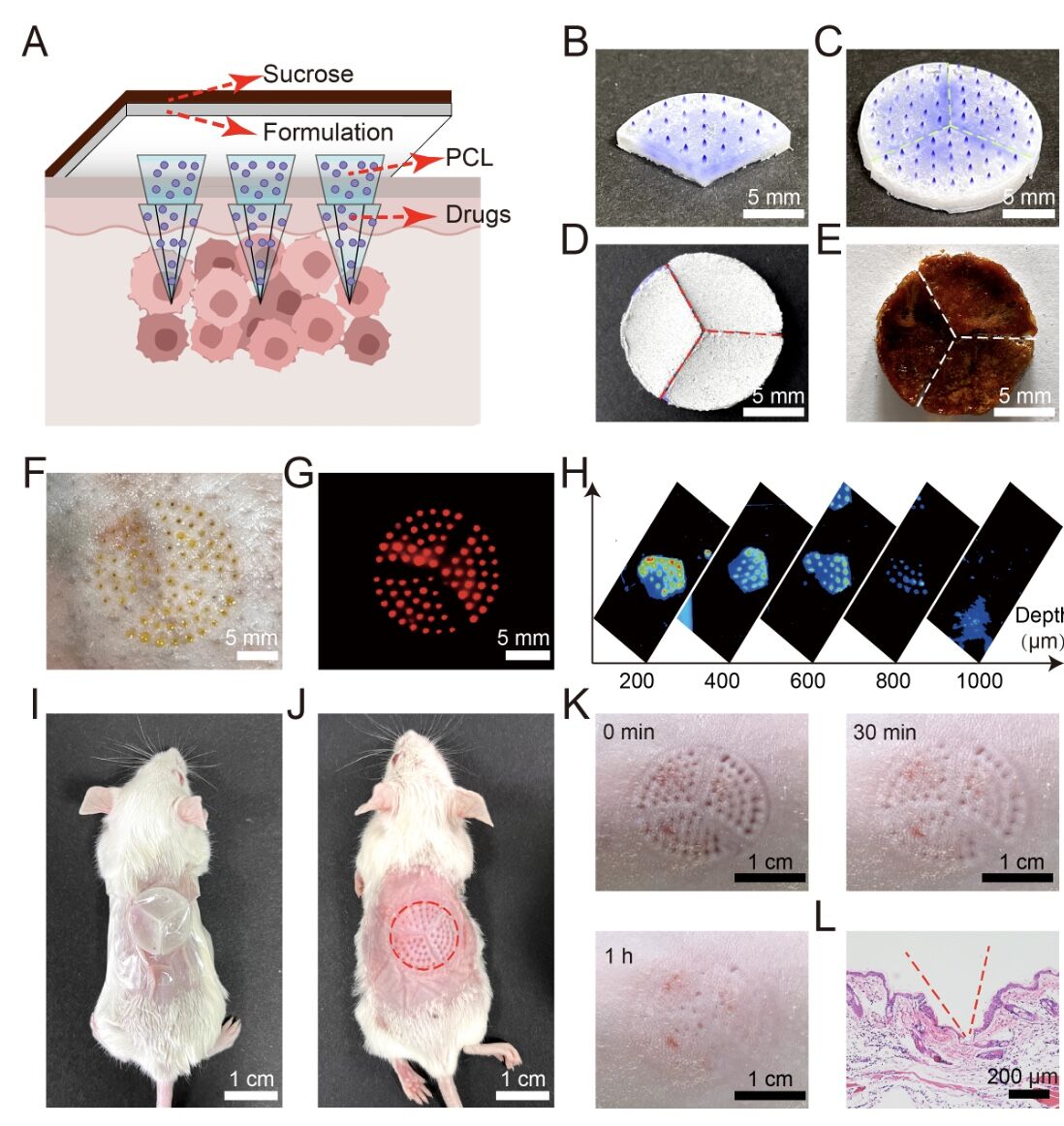
而此次使用药物是多烯紫杉醇,这是一种临床一线化疗药物,故能为后续的临床转化打下基础。同时,水热反应产生的产物是简单的无机盐,也能逐步被生物组织吸收,因此具备较好的生物安全性。需要指出的是,HRMAM系统的面世为人们提供了一种高效的深层递药系统,不仅在难以触及皮下肿瘤的治疗中展现出较大潜力,并展现出深层渗透、时空可控性、个性化适应性等特点,故有望用于需要高效局部给药的病症治疗之中比如糖尿病、皮肤病、风湿病等。
日前,相关论文以《智能水热反应微针用于局部肿瘤治疗》(Smart hydrothermally responsive microneedle for topical tumor treatment)为题发在 Journal of Controlled Release 上(IF 10.8),许仁珪是第一作者,陈伟担任通讯作者之一。华中科技大学同济医学院附属协和医学王琳主任和王征医生共同担任通讯作者。基于这一体系,以及华中科技大学同济医学院附属同济医院与协和医院的资源,课题组即将与临床医生开展合作,进一步推进HRMAM系统的临床转化。
