近日,我系陈伟教授团队结合了微针装置的光动力疗法在多种应用场景中提供较好的治疗效果,其安全性和便利性得到保证,为癌症治疗提供了新的选择。相关论文以《利用微针装置输送聚集诱导发光的光敏剂以增强癌症的节律性光动力疗法》(Microneedle Device Delivering Aggregation-Induced Emission Photosensitizers for Enhanced Metronomic Photodynamic Therapy of Cancer)为题发表在专业期刊《ACS Applied Materials & Interfaces》上(IF = 10.4),基础医学院药理学系徐家荣是共同第一作者,陈伟教授担任通讯作者之一。华中科技大学同济医学院附属同济医院王世宣教授和中国地质大学夏帆教授共同担任通讯作者。

光动力治疗(Photodynamic Therapy, PDT)是一种利用光敏剂在高强度、短时间的特定波长光照射下产生活性氧(Reactive Oxygen Species, ROS),从而杀死癌细胞的治疗方法。但是,常规的PDT在临床试验中没有达到预期的效果,与现有的治疗技术相比仍然不尽如人意。近年来,出现了一种新的PDT模式,即节律性光动力疗法(Metronomic Photodynamic Therapy, mPDT),它指的是使用低强度、长时间的光源进行治疗。多项研究证实,与常规PDT相比,mPDT具有更好的治疗效果,显示出更好的应用前景。然而,这种治疗方法目前仍面临着光敏剂的淬灭敏感性高和药物传递困难、需要反复给药等困难。
为克服上述挑战,陈伟教授在之前生物医用器件领域的基础上,开发了一种基于微针贴片的新型治疗策略。该方法结合了聚集诱导发光(Aggregation-Induced Emission, AIE)光敏剂的抗光淬灭性和微针的深层传递能力。通过这种方式,可以在长时间光照射后仍保持优越的光敏性,同时实现光敏剂在肿瘤中的均匀和深层分布,从而通过提高光敏剂递送效率和增强光动力治疗效果来有效抑制肿瘤生长。

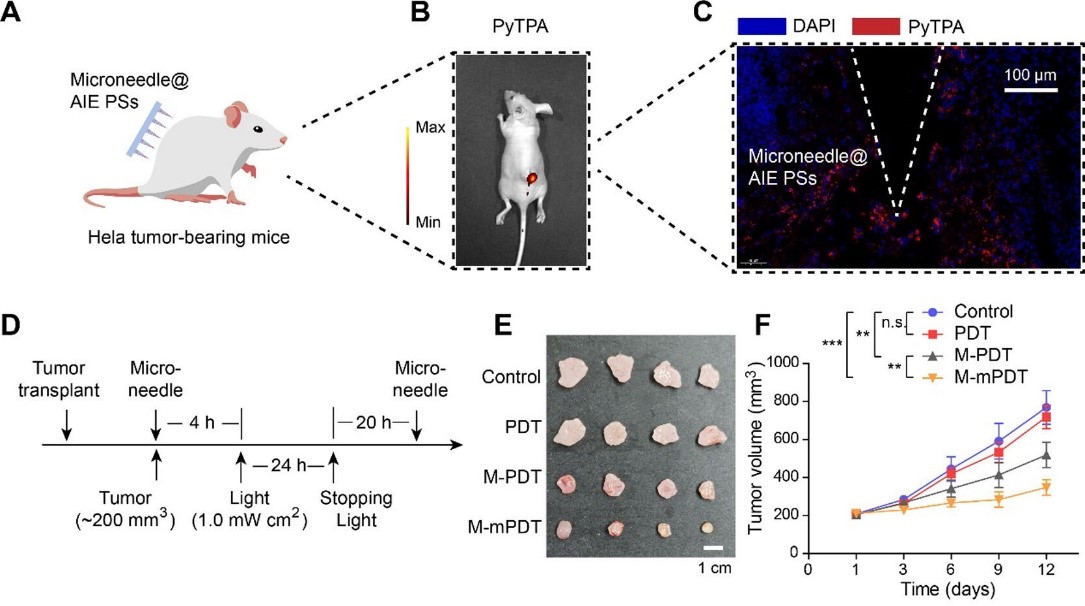
此次使用的微针材料主要是羧甲基纤维素(Carboxymethyl Cellulose, CMC),这是已被美国食品药品监督管理局(Food and Drug Administration, FDA)审批通过的生物医用材料。微针中加载的光敏剂是PyTPA,一种本研究团队之前已经证明的聚集诱导发光光敏剂。负载光敏剂的微针贴片可以通过光学显微镜和扫描电子显微镜观察其形貌。由于PyTPA具有良好的荧光信号,因此可以通过共聚焦激光扫描显微镜确定PyTPA被封装在微针中并具有良好的均一性。

利用小动物成像仪和共聚焦激光扫描显微镜,可以明显观察到经过微针贴片作用的小鼠肿瘤组织中聚集诱导发光光敏剂的均匀分布。动物实验结果表明,经过特定时间的光照处理后,结合了微针给药系统和聚集诱导发光光敏剂的新型治疗方法,不仅克服了光敏剂递送困难、分布不均匀的问题,而且通过微针穿刺通道增强了光源的组织穿透深度并且减少了光敏剂的淬灭,显著提高了mPDT的治疗效果,展现出更好的体内应用潜力。
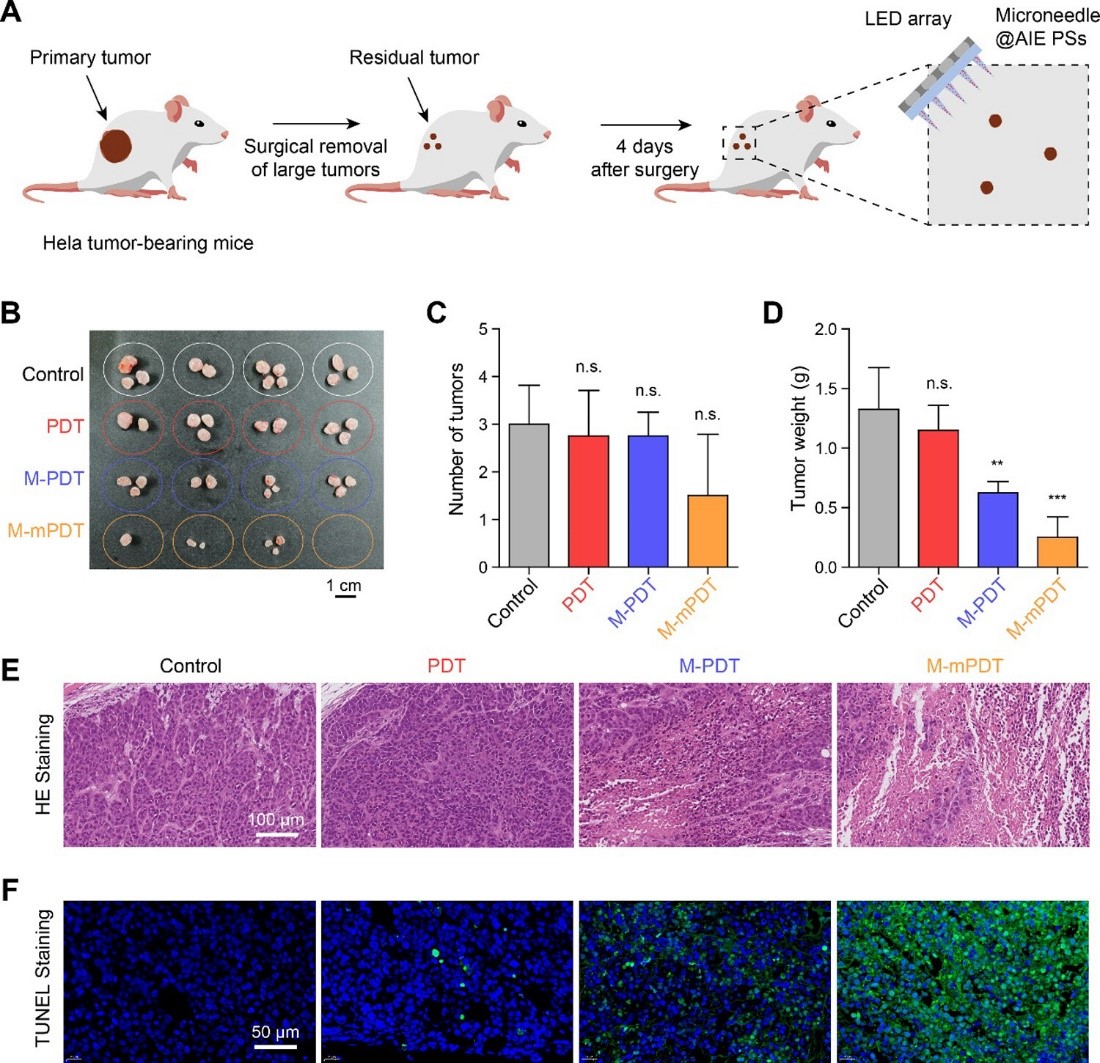
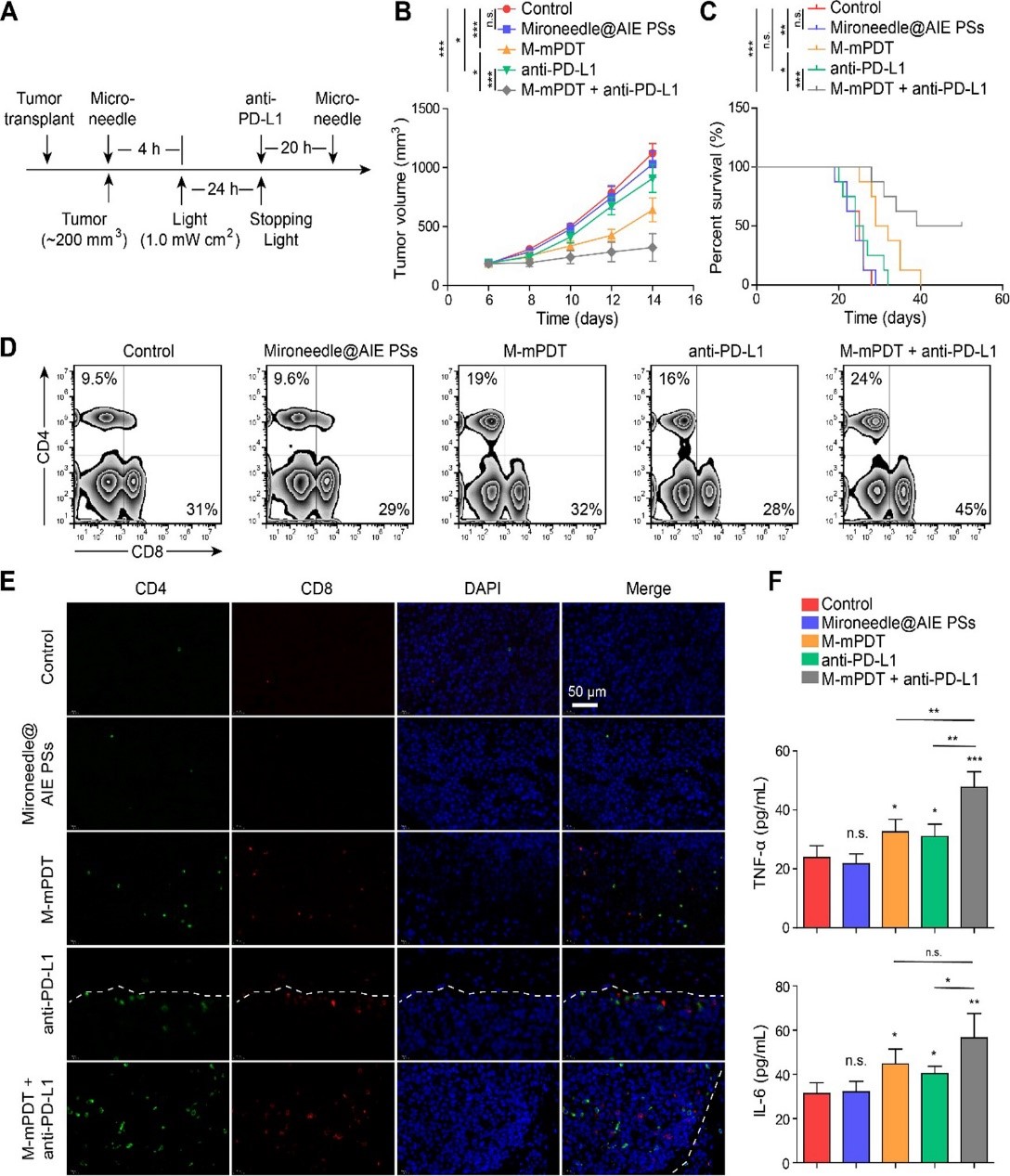
除了抑制体内肿瘤生长,负载光敏剂的微针贴片还能有效减少肿瘤术后的复发风险(上图)以及增强抗PD-L1免疫疗法的疗效(下图)。实验结果表明,微针贴片具有可调节的应用面积、微针密度和良好的穿透性,即使在残余肿瘤不可见的情况下也能有效地将光敏剂递送到肿瘤中,显著提高了mPDT的治疗效果。而在协同增强抗PD-L1免疫疗法的疗效实验中,可以发现当负载光敏剂的微针贴片和抗PD-L1联合使用时,肿瘤抑制效率进一步提高。这表明其可以显著增强抗PD-L1的疗效。
论文链接:
https://pubs.acs.org/doi/10.1021/acsami.3c01682