缺氧是糖尿病感染创面、恶性肿瘤及运动后乳酸堆积等多种疾病恶化的“幕后推手”。氧分压长期不足迫使细胞由有氧代谢转向低效的无氧糖酵解,乳酸累积、局部酸化并激活 HIF-1α 信号,最终抑制胶原合成、上皮化、免疫反应与血管生成,导致炎症持续、组织修复受阻。高压氧治疗虽能快速升高组织含氧量,却受制于昂贵设备、专业操作及氧毒性、气压创伤等风险,患者依从性差。近年来,微藻利用光合作用实现可持续产氧的优势受到关注,但其临床转化仍受植入安全、无菌保障、光照与养分依赖及难以精准定位/移除等问题掣肘。如何在避免高压氧疗弊端的同时,破解藻基供氧的生物安全与稳态控制难题,开发一种安全、便携、可持续的精准供氧技术,已成为跨学科亟待攻克的关键挑战。
华中科技大学基础医学院陈伟教授团队在《ACS Nano》发表最新研究成果"Self-Powered Algae-Integrated Wearable System for Oxygen Supplementation in Hypoxic Disease Treatment"(DOI: 10.1021/acsnano.5c02581),构建了一款基于摩擦纳米发电机(TENG)的自供能藻类集成可穿戴系统。该装置通过捕获人体运动机械能为发光二极管(LED)供能,精准调控微藻光合作用产生溶解氧,并将柔性封装舱与耐热基质巧妙融合,形成三大核心亮点:
1.自供能功能:TAPED 采用摩擦电纳米发电机(TENG)将人体运动转化为电能,驱动 LED 提供光照以激活藻类光合作用,无需外部电源,即可按需持续产氧。
2.安全藻类封装:微藻被封装在柔性外部腔室内,与组织完全隔离,避免直接植入可能引发的免疫反应或感染风险。
3.可控氧气释放:装置配备可调节氧气释放口,可将氧气精准输送至不同深度的缺氧组织,实现高效充氧与靶向治疗,提升整体疗效。
小鼠糖尿病感染创面模型中,无药物条件下使用TAPED治疗,9 天即实现创口完全闭合;在乳腺癌4T1模型中,与化疗药多西他赛联合可将肿瘤抑制率提高至77%;于大鼠运动疲劳模型中,局部乳酸含量降低约25%。TAPED轻质柔性、无需外部充电,且外封设计避免了微藻与组织直接接触的安全隐患,为多场景临床转化奠定基础。
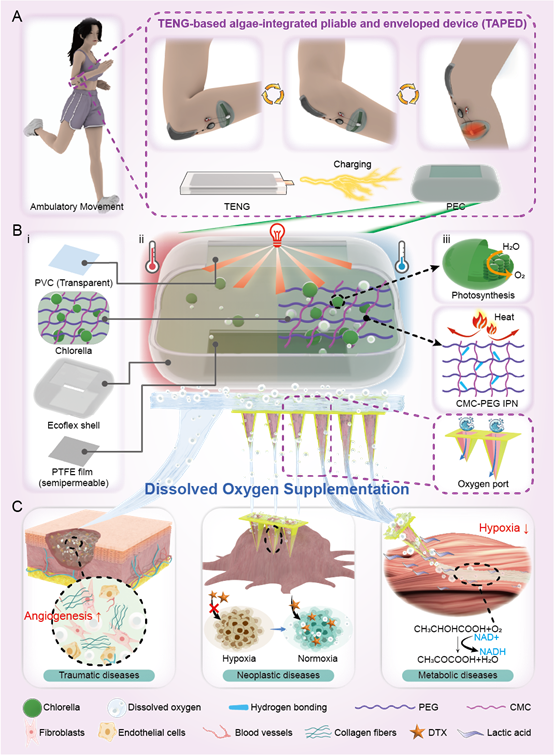
图1 TAPED系统原理与多功能应用:(A)TAPED系统通过人体机械运动收集能量;(B)柔性封装结构及可调节的氧气释放口实现稳定氧渗透;(C)糖尿病伤口、肿瘤缺氧及乳酸堆积三大应用场景。
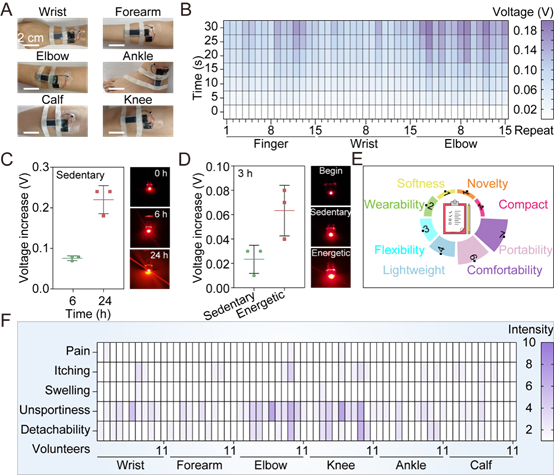
图2 TENG能量转换驱动LED发光强度提升与佩戴评估:(A)将自充电电容系统固定于志愿者的手腕、前臂、肘关节、踝关节、小腿和膝关节。(B)手指、手腕与肘关节持续弯曲时,3.3 μF电容的充电曲线。(C)静息状态下,TENG对钮扣电池充电6 h与24 h的累积电压(右侧为LED驱动器照片)。(D)静息与运动状态下,TENG充电3 h的钮扣电池累积电压对比。(E) TENG-LED贴片的使用倾向评价。(F)志愿者对TENG自供电系统佩戴舒适度的评价。
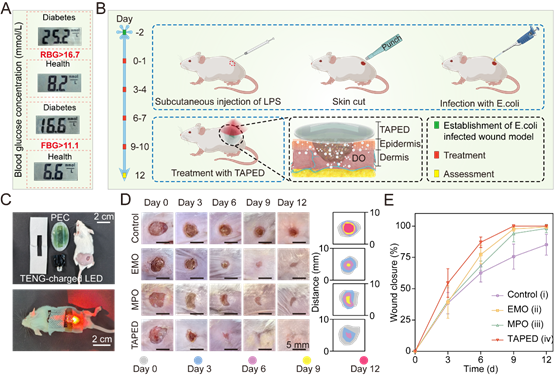
图3. TAPED系统促进体内细菌感染的糖尿病伤口愈合:(A)健康小鼠和糖尿病小鼠的随机血糖(RBG)和空腹血糖(FBG)水平。(B)建立感染大肠杆菌的糖尿病慢性伤口模型,以及使用TAPED治疗小鼠伤口的流程示意。(C)将TAPED系统应用于小鼠伤口并调节光合作用。(D)对照组、EMO组、MPO组和TAPED处理组在感染伤口愈合第0、3、6、9和12天的伤口图像,n = 5。12天内各组伤口面积示意图。(E)伤口愈合过程中伤口闭合率的定量分析,n = 5。
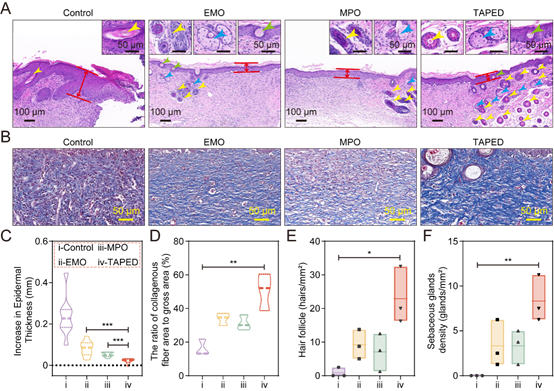
图4. TAPED治疗后伤口愈合的组织学评估。(A)使用苏木精-伊红(H&E)染色对伤口组织进行组织学分析。黄色箭头表示毛囊,绿色箭头表示角化,蓝色箭头表示皮脂腺,红色区域表示表皮厚度。(B)对第12天愈合的皮肤伤口进行Masson三色染色。对第12天表皮厚度增加(C)胶原纤维面积与总面积之比(D)、毛囊数量(E)和皮脂腺(F)进行量化(Students’T检验,*p < 0.05,**p < 0.01,***p < 0.001,n = 3)。
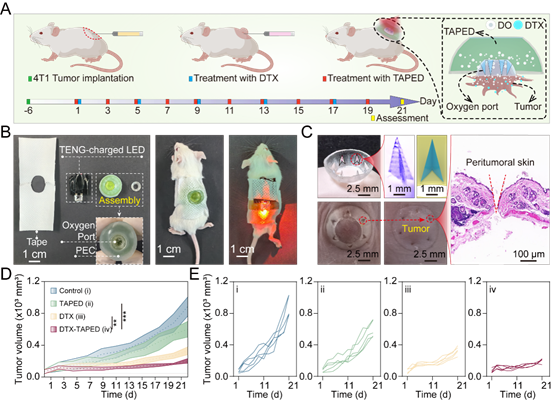
图5.基于TAPED的活体乳腺癌模型治疗。(A) 4T1乳腺癌模型的治疗示意图。(B)将TAPED系统应用于小鼠肿瘤并调节光合作用。(C)氧气端口及其应用于肿瘤的详细示意图,以及移除TAPED后BALB/c小鼠皮肤切片的病理H&E染色。(D)不同处理后4T1肿瘤的平均生长曲线(Students’T检验,**p < 0.01,***p < 0.001,n = 5)。(E)单个肿瘤生长曲线。
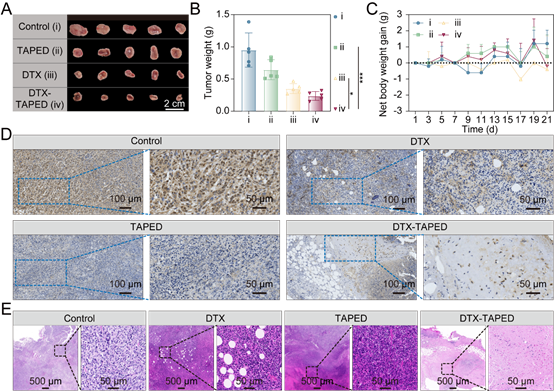
图6. TAPED对4T1肿瘤小鼠的疗效。(A)各组收获的肿瘤。(B)第21天各组肿瘤重量。(C)各组小鼠的净体重增加。(D)各种治疗后第21天收集的4T1肿瘤切片上HIF-1α的免疫组化染色。(E)不同治疗后第21天收集的4T1肿瘤切片的H&E染色。
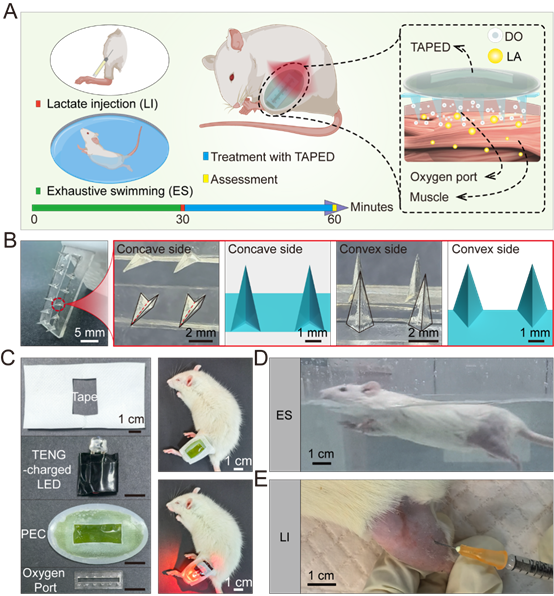
图7. TAPED系统减轻运动引起的乳酸堆积。(A)乳酸(LA)蓄积模型中的治疗计划示意图(使用BioRender.com创建)。(B)氧气端口针头的详细视图,说明凹面和凸面,液体更容易沿着凹面渗透。(C)在SD大鼠身上应用TAPED系统。(D)通过竭力游泳(ES)建立LA积聚模型。(E)通过在腿部注射LA (LI)建立LA积聚模型。
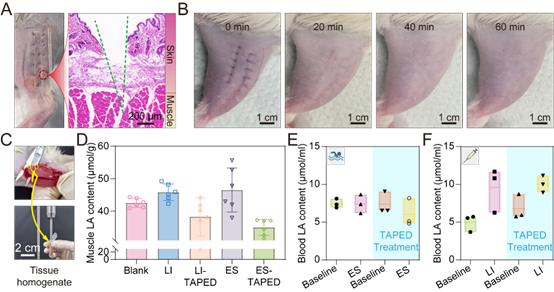
图8. TAPED处理的组织反应和乳酸调节。(A)氧气端口插入和拔出后SD大鼠皮肤和肌肉切片的H&E染色。(B)拔出氧气口后不同时间点的皮肤恢复情况。(C)组织收集和均质化过程。(D)不同组大鼠肌肉中的LA含量。(E)经TAPED处理和未经TAPED处理的ES组大鼠血液中LA含量。(F)经TAPED处理和未经TAPED处理的LI组大鼠血液中LA含量。
综上,TAPED以摩擦电自供能驱动LED、利用藻类光合作用持续产氧,并通过可穿戴外封设计实现安全、精准的氧气递送,在糖尿病创面愈合、肿瘤增敏治疗和运动后乳酸消除等模型中均展现出显著疗效;互穿聚合物网络(IPN)的引入保证了藻细胞活性和氧渗透效率,使该系统在无需外部充电的条件下即可长期稳定工作,提供了一条便捷、可持续且安全的缺氧疾病治疗途径。未来,研究团队将通过整合光伏和热电等混合能量模块提升续航,采用可替换低成本组件和模块化藻舱简化维护,结合多尺寸人体工学基座提高佩戴舒适度,并将装置纳入个体化康复护理方案,以期加速TAPED从实验室走向临床与运动康复现场,成为应对缺氧相关疾病的全新自供能治疗装备。
原文链接 https://pubs.acs.org/doi/10.1021/acsnano.5c02581