研究背景
现有镇静药物递送主要依赖静脉注射,引发的疼痛和焦虑限制了其在患者群体的应用,尤其是配合度低的儿童。滴鼻给药虽然避免了针头恐惧,但仍存在药物吸收稳定性差、易出现咳嗽等不良反应的局限。微针作为一种微创无痛的药物透皮递送策略,在镇静药物递送的创新方案中展现出巨大潜力。

研究
针对以上挑战,华中大基础医学院药理学系陈伟/刘慧研发了一种基于焦化蔗糖的新型微针系统——CALM。通过蔗糖焦化工艺的精细调控,克服传统糖基微针强度不足、稳定性差的瓶颈;创新地在微针表面引入开尔文晶胞结构,以增大比表面积,提高药物递送效率;此外,自主研发按压式操作辅助器,实现微针贴片过程的简便化、规范化操作,牢固贴合皮肤。搭载右美托咪定CALM系统在小鼠中呈现稳定的镇静效果,并在12名健康受试者中验证了安全性和舒适性。研究成果以“Swift-acting structured lattice-enhanced caramelized sucrose system for painless sedative delivery”发表在《Biomaterials》上。华中科技大学同济医学院基础医学院博士研究生梁欣婷、华中科技大学同济医学院附属协和医院麻醉医生杨磊、华中科技大学同济医学院临床八年制陈秀丽为共同一作,华中科技大学同济医学院药理学系陈伟教授、刘慧副教授为共同通讯作者。
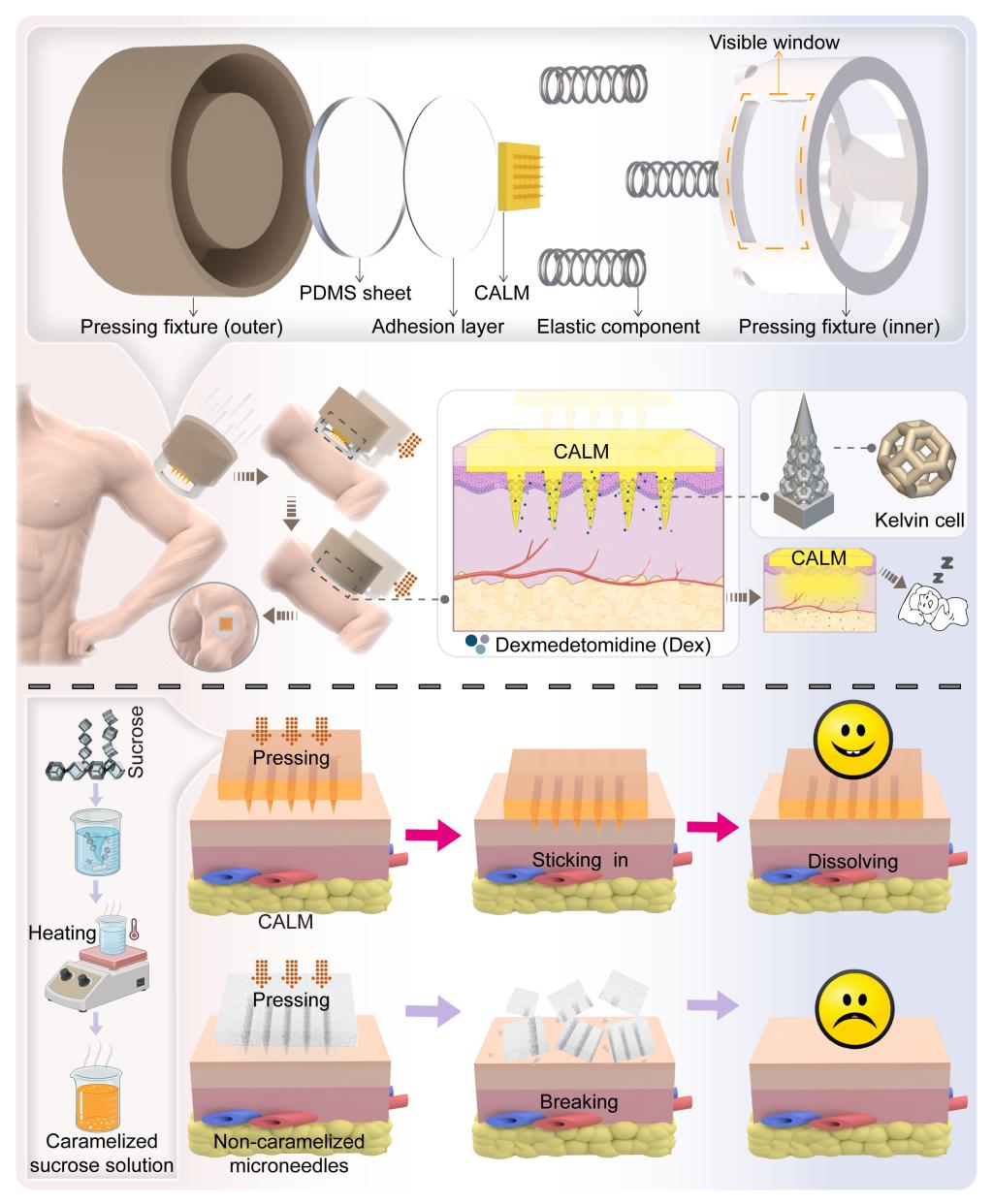
焦糖基结构化速效型微针贴片系统(CALM)实现镇静剂无痛递送
创新点1:焦化蔗糖无定形基质用于微针制备
糖基微针具有溶解速度快、生物安全性好的优势,但其机械强度差,且容易吸潮结晶,稳定性差。本研究通过精细调控焦化工艺(加热至180℃形成深黄色溶液),降低结晶度,形成无定形结构。该阶段焦化产物主要为单糖、二糖和低聚糖,不产生有毒物质;基于焦化蔗糖的微针储存2天后无结晶,插入皮肤时无断裂,显著增强了其稳定性和机械强度。

焦化前后机械强度对比
创新点2:开尔文晶胞结构设计增强微针药物递送效率
开尔文晶胞是一种由四面体和六面体组成的复杂凸多面体,最大限度地增大了比表面积。本研究通过在微针表面引入开尔文晶胞作为结构化修饰,有效增大微针与生物组织之间的接触面积,从而增强药物递送效率。通过有限元仿真,修饰开尔文晶胞结构的微针相较无结构微针,或修饰四面体、六面体的微针,显著增强了递效率。随后对开尔文晶胞层数进行详细优化,研究得出四层晶胞结构的微针溶解速度和药物递送速率最快,在离体猪皮中溶解时间仅为120秒。搭载荧光分子FITC作为模式药物,CALM系统载药分布主要在修饰有晶胞结构的外层,实现高效的药物透皮递送。

未修饰(左)和修饰(右)开尔文晶胞的溶解速度对比
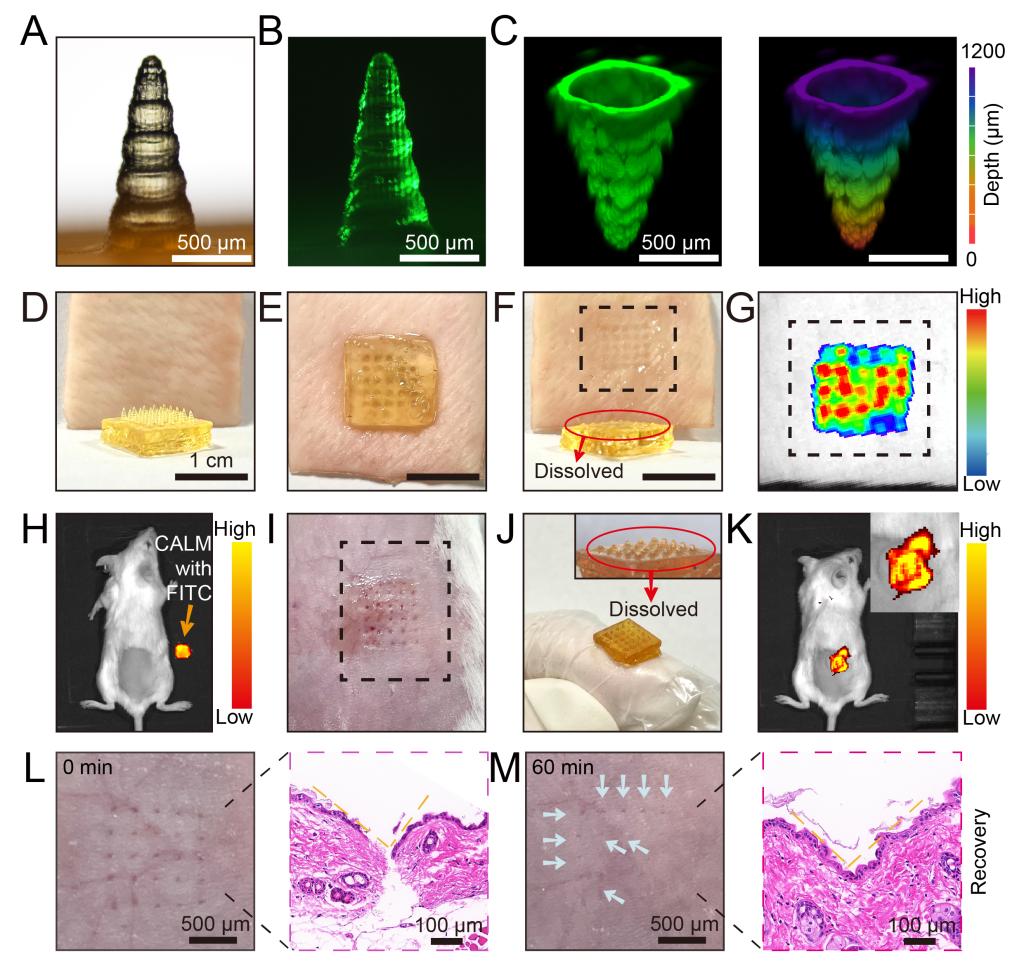
CALM系统的药物搭载和透皮递送
创新点3:按压式辅助器实现微针贴片便捷操作及牢固黏附皮肤
常规微针贴片通过拇指按压完成,存在施力方向不垂直、施力大小不均匀、粘附力差容易脱落的局限。本研究自主研发了按压式微针贴片辅助器,由外/内按压夹具、PDMS层、黏附层和弹性组件构成。该辅助剂仅需通过简单按压即可完成操作,确保微针与皮肤紧密贴合,避免移位,同时预留了观察窗口以确保操作安全。
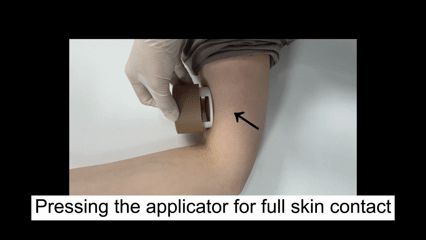
按压式辅助器的操作过程
应用成效1:在小鼠中实现稳定镇静效果
小鼠经CALM递送右美托嘧啶后,5分钟内血浆药物浓度达峰值(16.56ng/mL),镇静效果持续约70分钟,与皮下注射、静脉注射疗效相当,优于滴鼻给药。
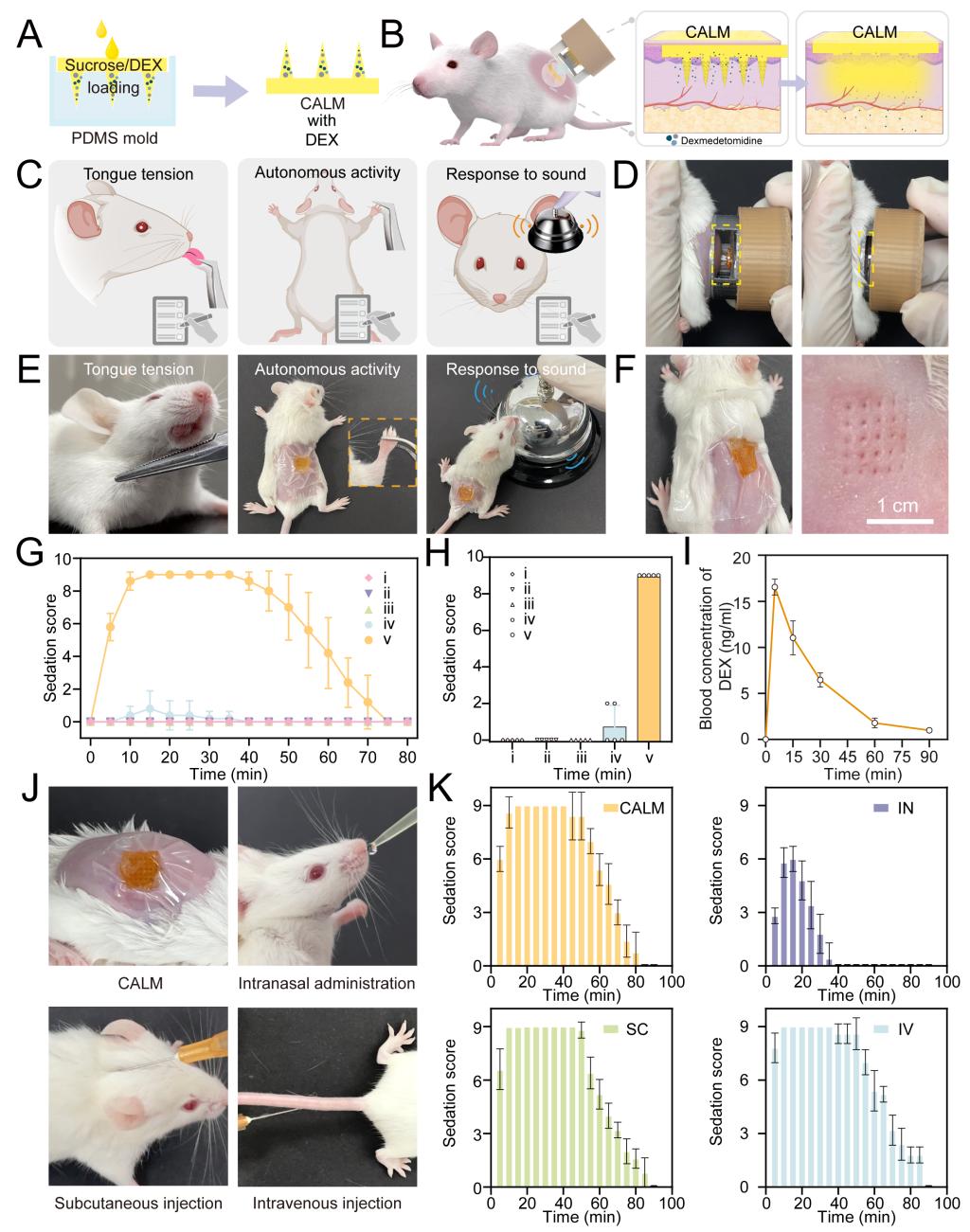
搭载右美托嘧啶的CALM系统在小鼠中的镇静效应
应用成效2:健康受试者中的安全性及舒适性评价
在严格的无菌操作下,麻醉医生为12名健康受试者使用了CALM系统,92%的人仅感受到轻微不适(疼痛评分1-2分),使用部位红斑2小时内消退,3小时完全恢复。受试者和操作者对CALM系统的舒适度、稳定性和操作便捷性满意度较高。
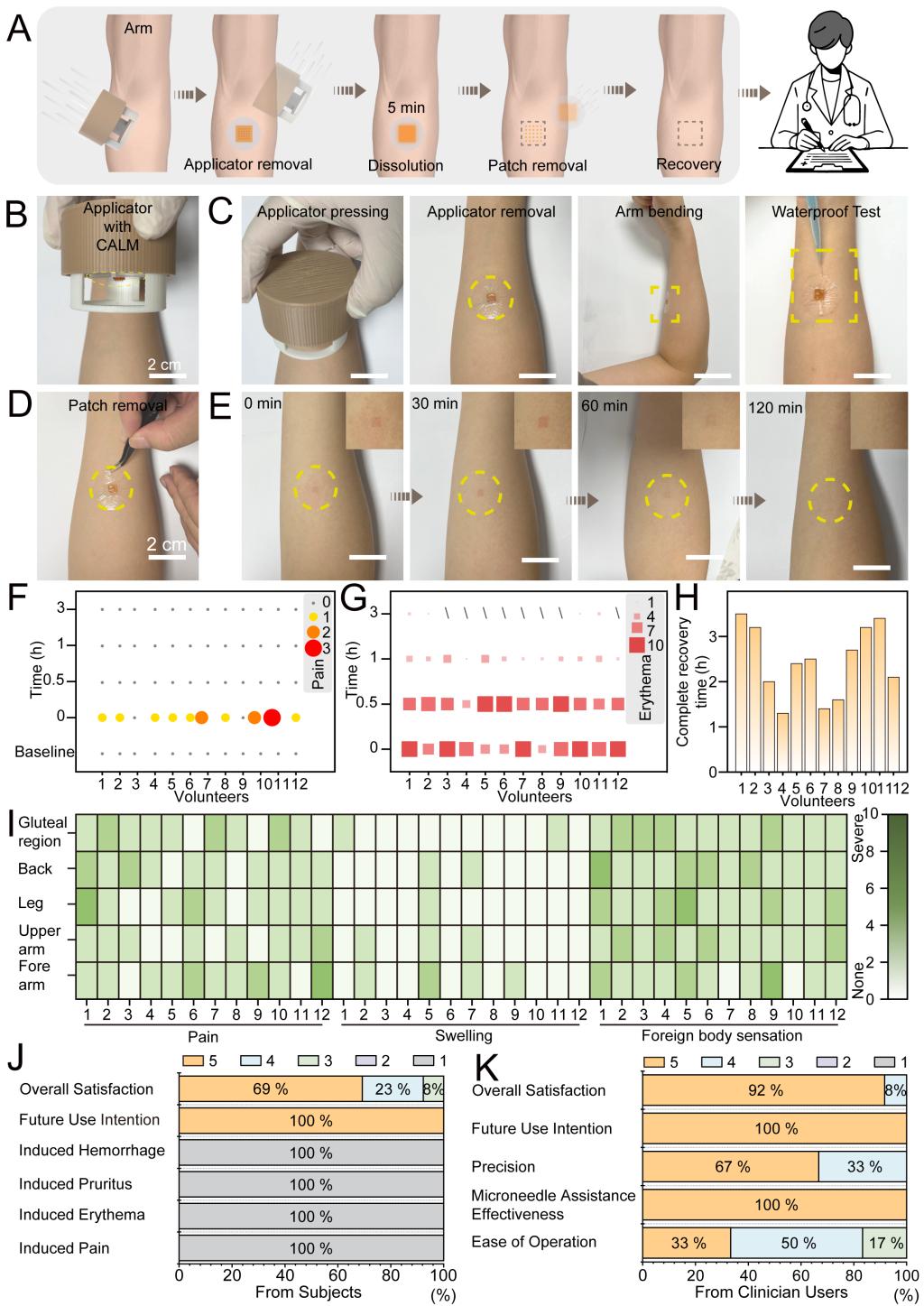
CALM系统在健康受试者中的应用
未来展望
CALM系统在镇静药物递送中具有舒适无痛、药物递送效率高、稳定性强的突出优势,在动物实验及早期临床试验中表现出色。接下来将开展更大规模的临床试验,加快其临床转化。
通讯作者介绍
华中科技大学同济医学院药理学系陈伟教授:博士生导师,国家海外高层次青年人才(2022),湖北省“杰青”(2022),湖北省“百人计划”(2021)入选者。陈教授2009年于武汉大学化学基地班专业获理学学士学位,2014年在浙江大学化学系获得博士学位。2015-2018年在美国国立卫生研究院National Institutes of Health(NIH)陈小元教授课题组从事博士后研究,2018-2020年于麻省理工学院(Massachusetts Institute of Technology, MIT)Robert S. Langer教授(美国三院院士,2021年增选为中国工程院外籍院士)课题组任研究科学家(Research Scientist)。2021年加入华中科技大学同济医学院基础医学院药理学系,任教授,兼任Chinese Chemical Letters和MedComm-Biomaterials and Application青年编委,以及Journal of Nanobiotechnology客座编辑。
华中科技大学同济医学院药理学系刘慧副教授:学系副主任,湖北省药理学会常务理事,“中国药理学会-施维雅青年药理学工作者奖”获得者,2003~2005年香港大学心血管研究所访问学者,2012~2014年香港大学李嘉诚医学院生理学系博士后人员。长期从事药理学的教学与科研工作,主持及参与多项国家自然科学基金、科技部科技攻关项目及省市级科研项目。
原文连接:Xinting Liang#, Lei Yang#, Xiuli Chen#, Yusheng Gong, Rengui Xu, Qi Zeng, Jiarong Xu, Jiajing Liu, Yuan Liu, Guanyue Li, Linxi He, Wenhao Jiao, Hui Liu*, Wei Chen*. Swift-acting structured lattice-enhanced caramelized sucrose system for painless sedative delivery.Biomaterials2025, DOI: 10.1016/j.biomaterials.2025.123823.
团队主页:https://wi13qnj3el.feishu.cn/docx/R3WFdsbAqoR0G4x6hJYcNYWvnoS