研究背景
结直肠癌(CRC)是全球第三大常见癌症,也是癌症相关死亡的第二大原因。当前的治疗手段,尤其是针对转移性CRC,仍面临化疗耐药、不良反应以及免疫治疗响应人群有限等严峻挑战。益生菌疗法因其安全性和调节肠道微生态的潜力备受关注,但其作为独立疗法的临床转化长期受困于两大瓶颈:口服后难以在肿瘤部位有效富集,以及在复杂的肿瘤微环境中生物活性不足,导致单用疗效不确切。
研究成果
针对上述挑战,华中科技大学同济医学院附属协和医院王征教授、王琳教授团队与基础医学院陈伟教授团队合作,创新性地提出了一种“金属离子工程化”益生菌策略。研究人员发现,锰离子(Mn²⁺)能显著增强罗伊氏乳杆菌(Lactobacillusreuteri)的增殖、甘油代谢及结直肠定植能力。基于此,团队通过化学修饰构建了锰工程化罗伊氏乳杆菌(MnLR),并将其与代谢底物甘油(Gly)联用,形成口服活体生物药(MnLR/Gly)。
该策略在多种临床前模型中展现出卓越的疗效:在原位结肠肿瘤模型中,单独口服MnLR/Gly实现了95.6%的肿瘤生长抑制率,并减少62.1%的肝转移;在预防性模型中,75%的小鼠长期无瘤,62.5%的小鼠成功抵抗肿瘤再挑战。机制上,MnLR/Gly不仅能直接杀伤肿瘤细胞,还能同时激活肿瘤局部及外周的抗肿瘤免疫(诱导树突状细胞成熟、M1型巨噬细胞极化、效应T细胞活化)。为推进临床转化,团队进一步开发了肠溶胶囊(GlyMnLR),在兔原位结直肠癌模型中验证了其与标准化疗相当的疗效及良好的安全性。相关成果以“Manganese-engineered Lactobacillus Reuteri with enhanced antitumor and immunomodulatory activities for colorectal cancer prevention and treatment”为题发表在《Nature Communications》上。华中科技大学同济医学院附属协和医院曹鹏博士、李琪琳博士为共同第一作者,王征教授、王琳教授、陈伟教授为共同通讯作者。

1从“代谢物”切入:直接抑瘤并重塑肿瘤免疫
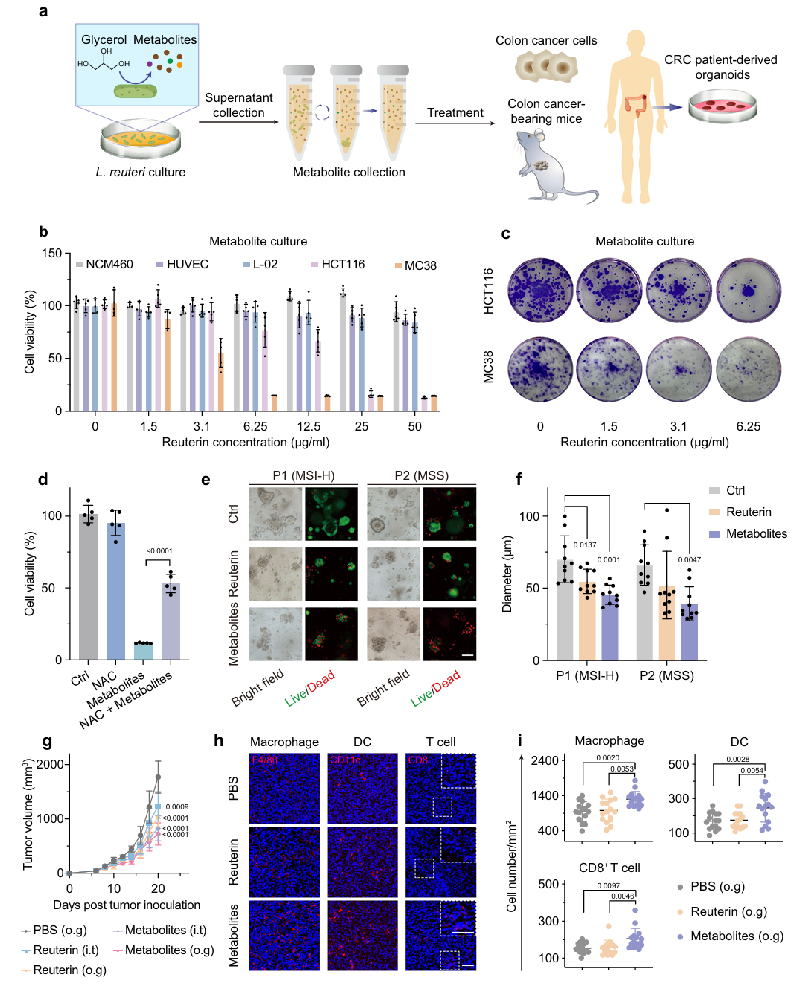
研究首先证实,罗伊氏乳杆菌代谢甘油产生的混合代谢物(以reuterin为主)对结直肠癌细胞具有选择性杀伤作用,且效果优于单一纯品reuterin。更重要的是,口服该代谢物不仅能抑制肿瘤生长,还能显著增加肿瘤微环境中巨噬细胞、树突状细胞和CD8⁺T细胞的浸润,提示其具有“直接杀伤”与“免疫激活”双重功能。
2.把益生菌“锰工程化”:MnLR的筛选、制备与表征
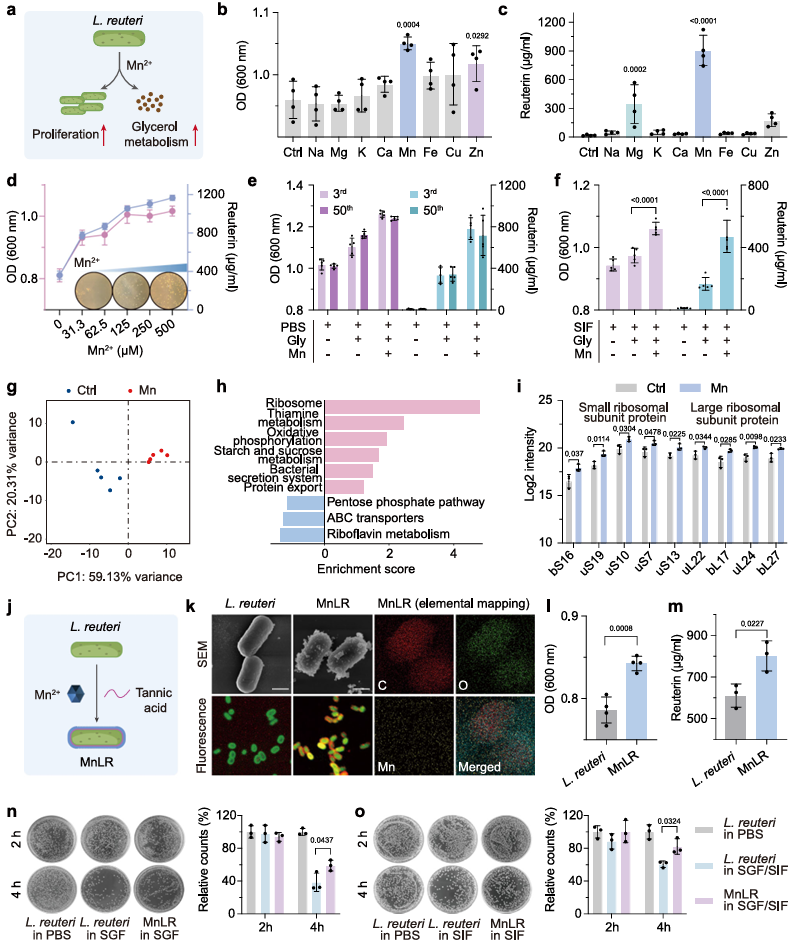
针对益生菌在体内活性不足的痛点,团队通过筛选发现Mn²⁺能同时促进罗伊氏乳杆菌的增殖与甘油代谢。通过单宁酸(TA)作为化学连接剂,成功将Mn²⁺修饰于菌体表面,构建了MnLR。研究表明,MnLR在模拟胃肠液中存活率更高、增殖能力更强、代谢产生活性物质(reuterin)更多,且在结肠肿瘤部位的定植量是未修饰菌的1.7倍。
3.双路径启动免疫:抑制癌细胞+促进树突状细胞成熟
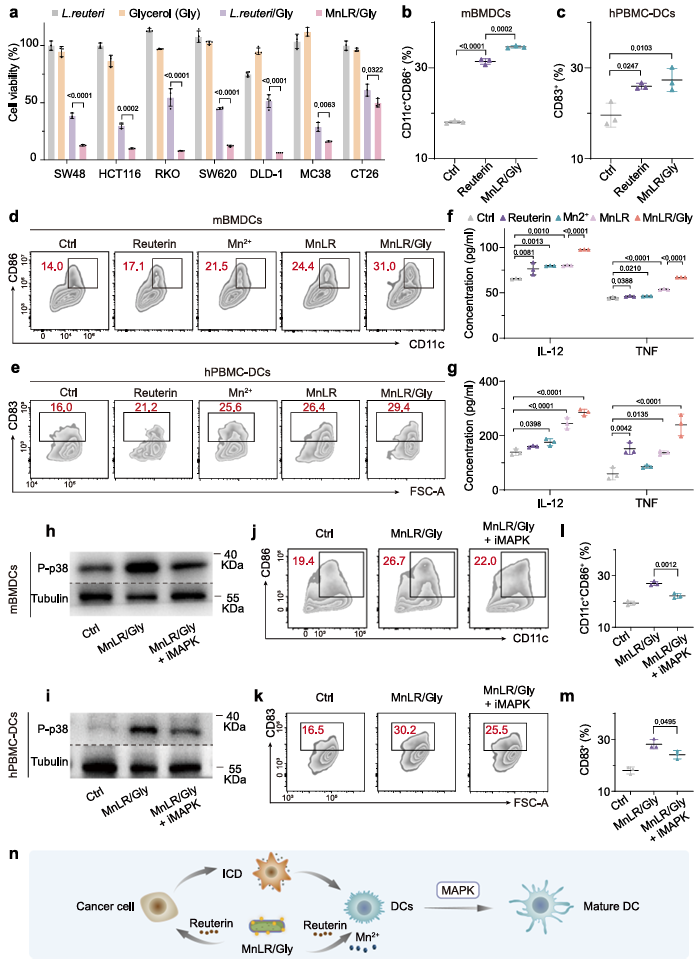
MnLR/Gly不仅能直接诱导肿瘤细胞发生免疫原性细胞死亡(ICD),释放“吃我”信号,其本身也能直接刺激树突状细胞成熟。体外实验显示,经MnLR/Gly处理的肿瘤细胞裂解物,或直接刺激树突状细胞,均能显著提高成熟树突状细胞比例及IL-12、TNF等免疫激活细胞因子水平。
4.把“巨噬细胞方向盘”拨向抗肿瘤:体外极化驱动免疫激活
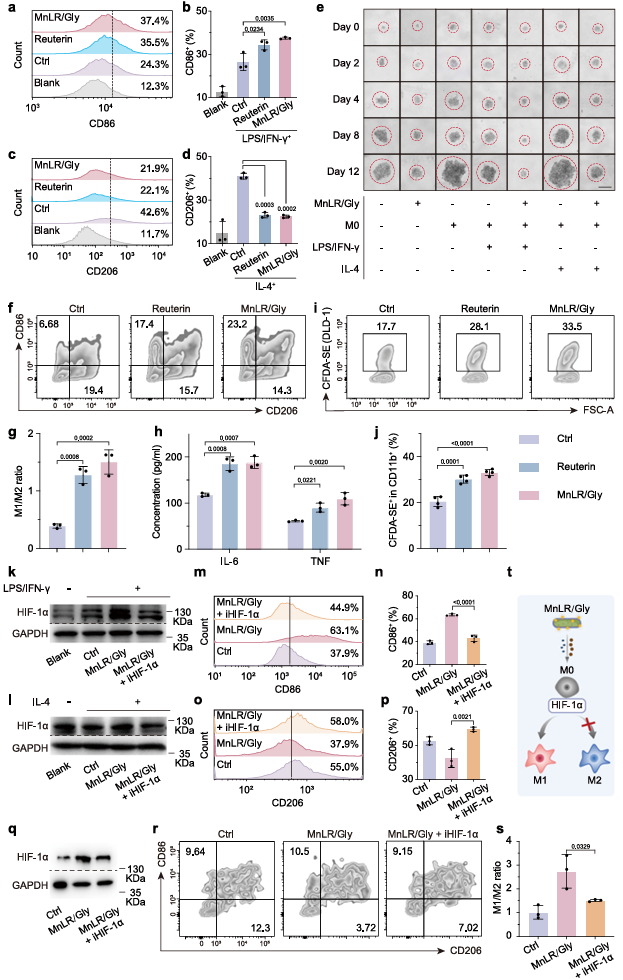
MnLR/Gly能够将巨噬细胞从免疫抑制的M2型“重编程”为抗肿瘤的M1型。在体外极化模型中,MnLR/Gly处理显著提高了M1型巨噬细胞标志物(CD86、iNOS)表达,降低了M2型标志物(CD206、Arg-1)表达,并增强了巨噬细胞对肿瘤细胞的吞噬能力。机制研究表明,这一过程部分通过调控HIF-1α通路实现。
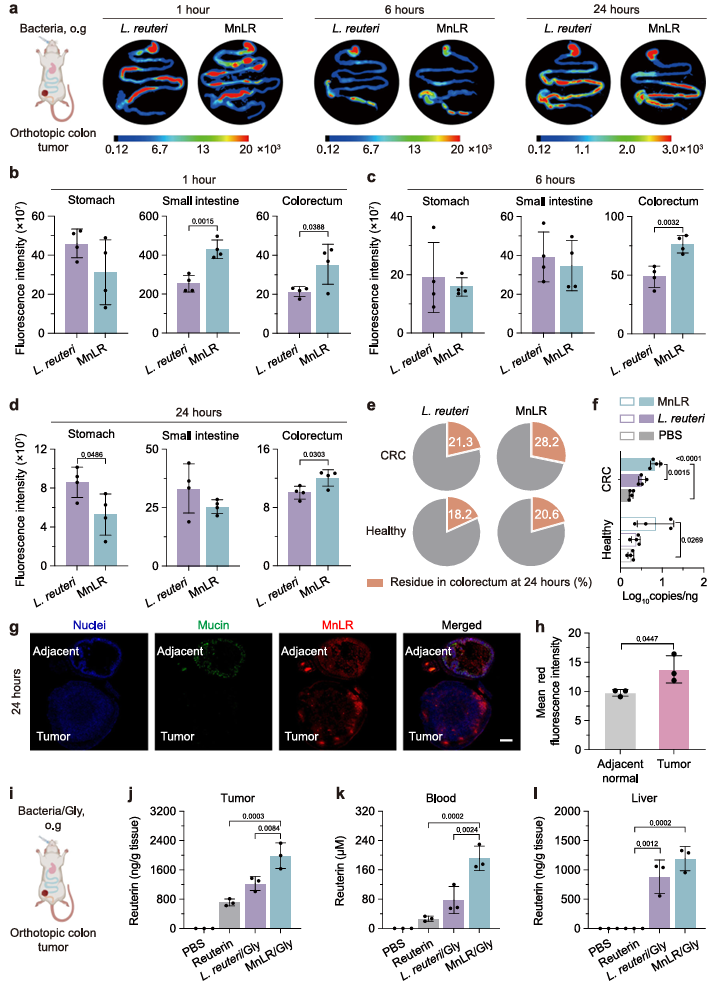
5.口服后的真实去向:体内动态分布与结肠定植
通过荧光标记和活体成像,团队追踪了MnLR在体内的命运。结果显示,口服后MnLR在结肠肿瘤部位的富集量是未修饰菌的1.7倍,且这种优势可维持至少24小时。更重要的是,MnLR在肿瘤组织中比邻近正常组织富集更多,并倾向分布于肝脏(结直肠癌常见转移部位)。LC-MS/MS检测证实,MnLR/Gly组在肿瘤组织中的reuterin浓度显著高于对照组。
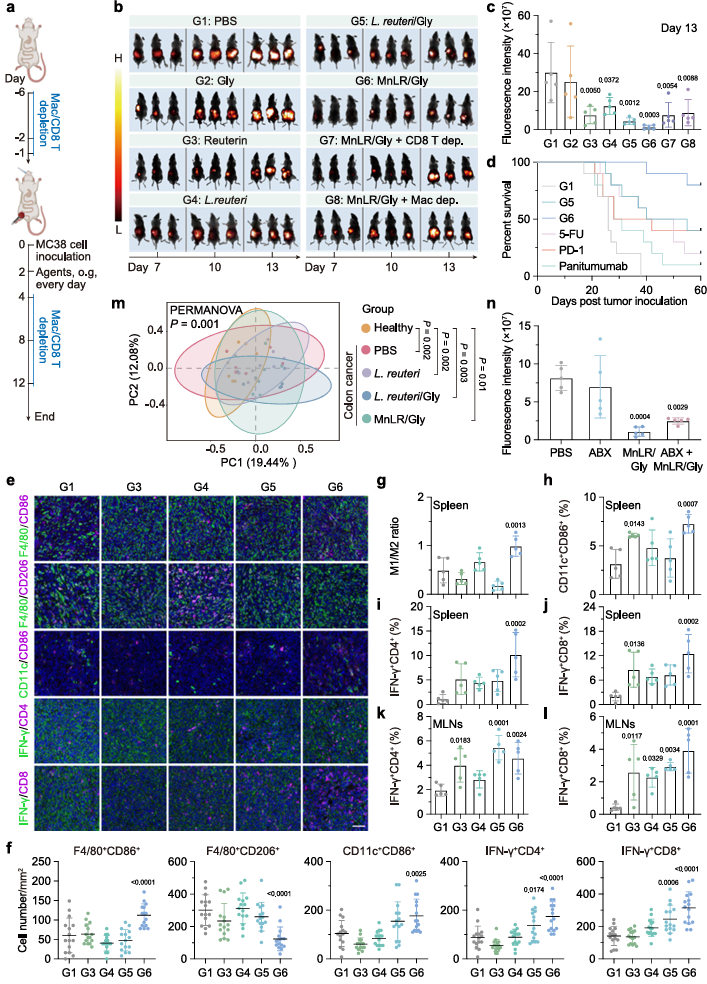
6.原位结肠癌模型三连击:抑瘤+菌群调控+抗肿瘤免疫激活
在原位结肠癌小鼠模型中,口服MnLR/Gly实现了95.6%的肿瘤生长抑制率,显著延长了小鼠生存期(80%小鼠存活超过60天),其疗效优于PD-1抗体、5-FU和帕尼单抗。机制层面,MnLR/Gly显著增加了肿瘤内M1型巨噬细胞、成熟树突状细胞及IFN-γ⁺CD4⁺/CD8⁺T细胞的比例,并部分改善了肿瘤诱导的肠道菌群失调。CD8⁺T细胞或巨噬细胞耗竭实验证实,这些免疫细胞是MnLR/Gly发挥抗肿瘤作用的关键效应细胞。
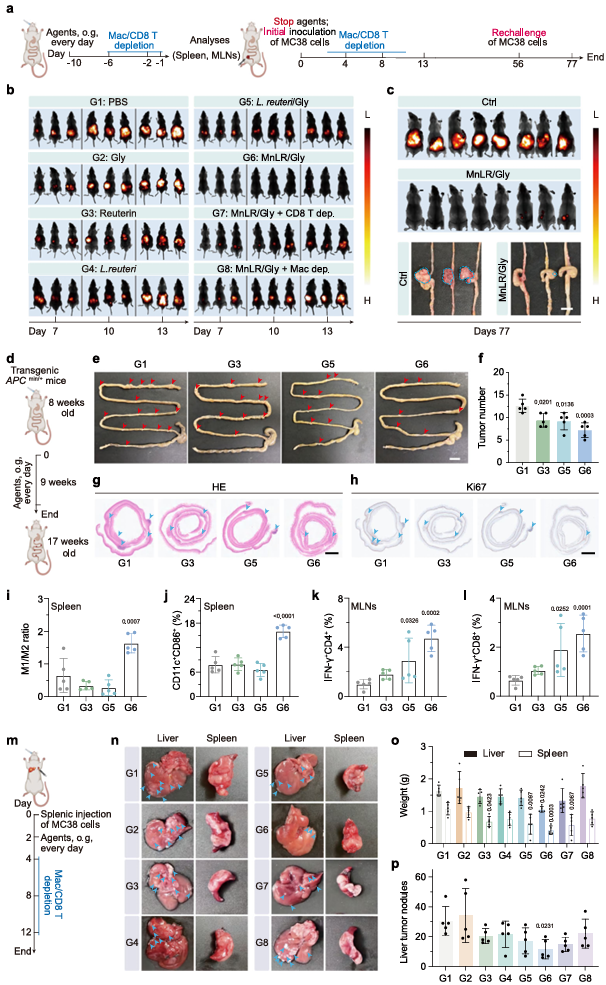
7.从治疗走向预防:阻断原发与转移
研究进一步探索了MnLR/Gly的预防潜力。在预防性给药10天后接种肿瘤细胞,75%的小鼠在8周内保持无瘤状态;对无瘤小鼠进行肿瘤再挑战,62.5%的小鼠依然无瘤,表明MnLR/Gly能诱导长期免疫记忆。在Apcmin/+转基因自发肠癌模型中,MnLR/Gly显著减少了肠道肿瘤数目和Ki-67阳性增殖细胞。此外,在肝转移模型中,MnLR/Gly使肝转移结节数减少62.1%,并显著降低了转移肝叶重量。
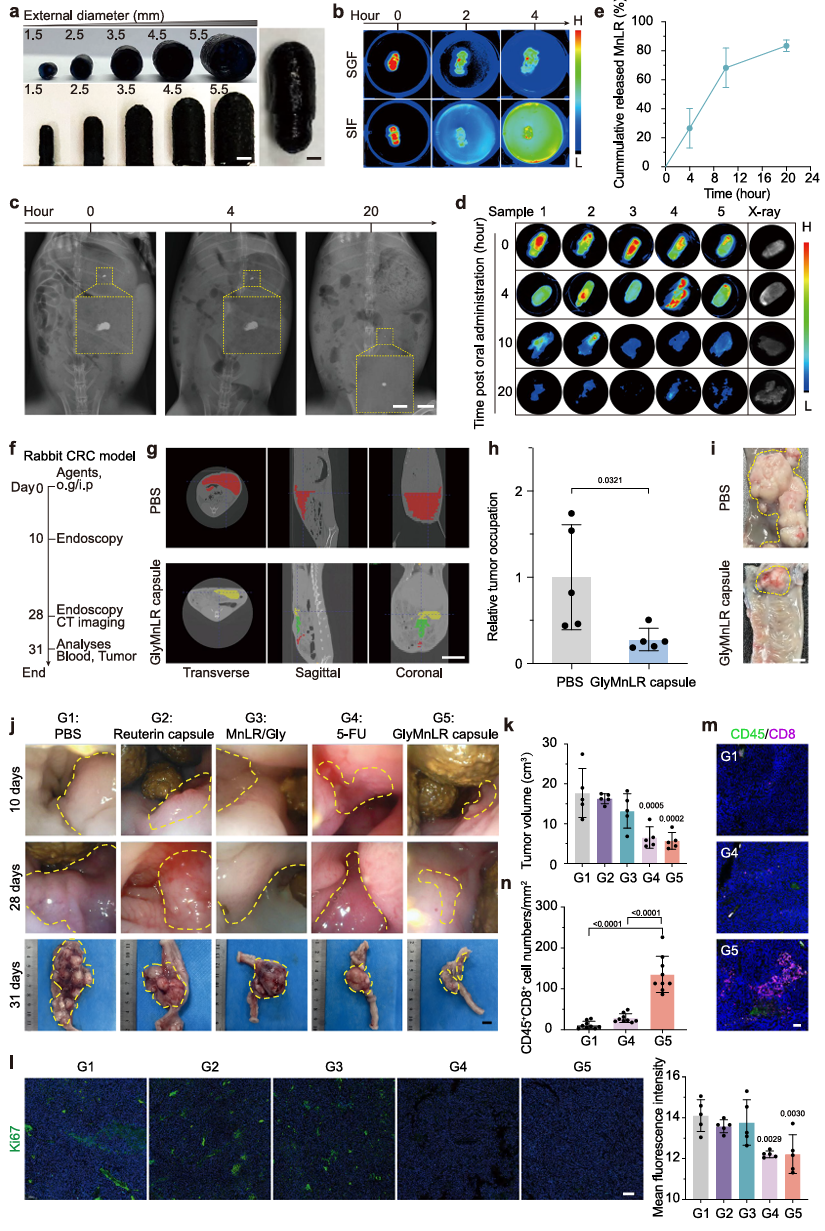
8.工程化递送闭环:胶囊化实现“持久且有效”的兔CRC治疗
为解决口服益生菌在胃酸环境中的活性损失,团队自主开发了GlyMnLR肠溶胶囊。该胶囊在胃中保持完整,到达肠道后迅速溶解,实现了MnLR与甘油在肿瘤部位的靶向共释放。在更具临床相关性的兔原位结直肠癌模型中,GlyMnLR胶囊的肿瘤抑制率达67.9%,疗效优于游离MnLR和reuterin胶囊,与一线化疗药5-FU相当,且未观察到明显毒副作用。免疫荧光显示,GlyMnLR胶囊显著增加了肿瘤组织中CD8⁺T细胞的浸润。
研究小结
本研究通过金属离子工程化策略,成功将传统益生菌升级为兼具“高效靶向”、“代谢杀伤”与“免疫重塑”功能的独立活体药物。MnLR/Gly不仅显著抑制了原发肿瘤的生长,还在预防肿瘤发生和转移方面展现出独特优势,为结直肠癌的全程管理提供了全新的“口服活体药物”范式。