创伤后应激障碍(Post-Traumatic Stress Disorder, PTSD)指个体经受或目睹突发性灾难事件后出现的严重应激障碍。病理性恐惧记忆的反复侵入与重现是PTSD的核心症状。到目前为止,PTSD的发生机制仍未被阐明清楚,临床上严重缺乏针对性的有效治疗药物。2024年10月9日,华中科技大学陈建国/吴鹏飞/王芳教授共同通讯在国际生物学领域权威期刊Redox Biology在线发表题为“Methionine oxidation of actin cytoskeleton attenuates traumatic memory retention via reactivating dendritic spine morphogenesis”的研究论文。该研究结果表明,基底外侧杏仁核(basolateral amygdala complex,BLA)脑区肌动蛋白细胞骨架的蛋氨酸残基酶促氧化通过促进树突棘骨架重塑、减弱创伤性恐惧记忆保持并促使其消退,为PTSD的治疗提供了新的潜在作用靶点。基础医学院2019级博士研究生黄存东为本文第一作者。

氧化还原修饰指由于蛋白质关键氨基酸残基的氧化还原状态变化引起的翻译后修饰,如形成二硫键、S-谷胱甘肽化、S-巯基化、S-亚硝基化、S-次磺酸化、蛋氨酸亚砜化等,在很多生理和病理生理过程中都发挥着重要作用。一般认为细胞内活性氧、活性氮、活性硫等化学性质活泼的氧化还原信号分子通过直接与蛋白质半胱氨酸、蛋氨酸等残基发生化学反应,介导氧化还原修饰的发生。陈建国/王芳/吴鹏飞团队长期围绕氧化还原信号分子对突触功能和结构可塑性的调控机制及其在神经精神疾病中的作用开展研究,前期系列工作(Aging Cell 2010, 2017; J Neurosci. 2014;Antioxidants and Redox Signaling 2015,2017,2019;Acta Pharm Sin B 2021;Acta Pharmacologica Sinica 2022;Redox Biology 2022等)已证实活性氧等氧化性分子所介导的蛋白质半胱氨酸等残基氧化在突触可塑性损伤和认知功能障碍中可能发挥重要作用。除通过与氧化性分子直接反应外,研究表明部分蛋白质的蛋氨酸残基可作为特异性的底物被体内某些蛋氨酸氧化酶催化氧化。CasLs相互作用分子1(MICAL1)是一种选择性氧化丝状肌动蛋白F-actin的蛋氨酸氧化酶,可立体专一性的将F-actin蛋白 44/47位蛋氨酸残基氧化为R型蛋氨酸亚砜(R-MetO),使其电性改变从而干扰Actin单体间的相互作用,促进F-肌动蛋白切割、解聚成G-actin,这种氧化可被蛋氨酸亚砜还原酶B1(MsrB1)选择性还原。到目前为,MICAL1介导的F-actin酶促氧化解聚在中枢神经系统中的作用还知之甚少。本研究发现,创伤性应激发生后BLA脑区蛋氨酸氧化酶MICAL1表达持续下调、而还原酶MsrB1表达上调,导致肌动蛋白F-actin的蛋氨酸氧化水平降低,肌动蛋白细胞骨架动力学向Actin聚合方向移动,引起树突棘骨架可塑性下降,最终导致恐惧记忆的持久保持。过表达MICAL1基因逆转创伤性应激引起的BLA脑区肌动蛋白装配和树突棘密度增加,减少小鼠恐惧记忆保持、促进恐惧记忆消退。通过持续性皮质酮饮入结合条件恐惧训练诱导小鼠PTSD样记忆模型发现,BLA脑区过表达MICAL1基因抑制皮质酮诱导的恐惧记忆习得增强;敲低MICAL1基因则模拟出皮质酮诱导的恐惧记忆消退障碍。
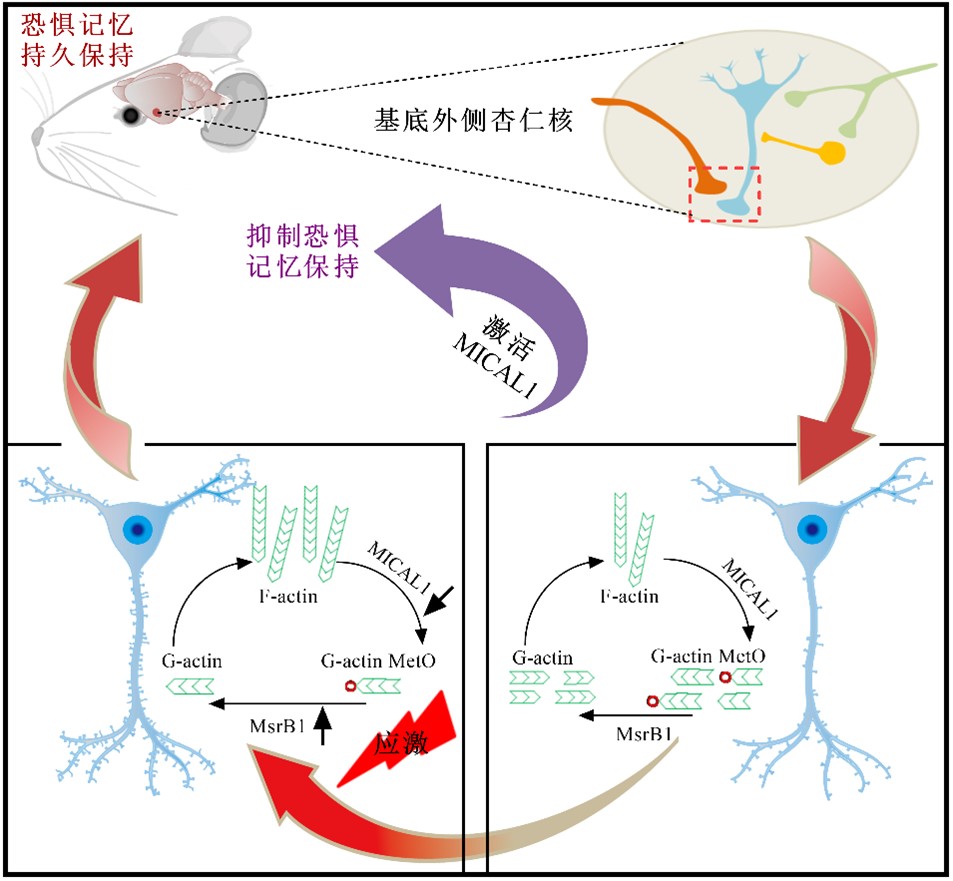
综上所述,本研究阐明了F-actin蛋氨酸氧化还原状态及其关键酶MICAL1等在恐惧记忆保持和消散中的作用,为靶向肌动蛋白细胞骨架治疗PTSD等负性情感记忆相关疾病提供了潜在的药物靶点。
(撰稿人 吴鹏飞)