口服给药方式目前仍然是病人依从度最高、应用最为广泛的药物递送途径,但由于消化系统中的多重生化、黏液以及上皮屏障,大分子(如蛋白质、多肽等)经由口服递送的效率十分有限。目前已有研究尝试研发各类技术方法针对不同吸收屏障进行干预,以促进大分子药物口服递送,包括渗透增强剂、酶抑制剂、细胞穿透肽、生物粘附分子、自组装气泡载体、纳米颗粒载体、自乳化给药系统、离子液体等。虽然部分体系已表现出增强大分子药物口服吸收的潜力,但仍然无法显著提高大分子药物的口服生物利用度。这是由于目前的策略无法快速有效地同时克服复杂多变的胃肠道生化、黏液和上皮等屏障所导致。微针技术的发展为大分子药物口服递送提供了全新的机遇。微针给药避开了常规口服制剂面临的多种挑战,可以借助其形成的微米尺度的传输通路(微创方式)直接将大分子药物递送到皮下组织。基于结构和材料优化,微针系统不仅可以大量担载大分子药物,保护药物到达靶点,并且在刺入上皮后快速溶解,释放药物,实现微创、高效、安全递送。然而,胃肠道肌肉的蠕动、沿胃肠道的渗透应力以及腔内胃液流速引起的剪切应力可能加速微针的脱落,进而使其失去作用,快速排出。此外,在到达靶点发挥作用前,微针也容易被消化液侵蚀,破坏结构,失去功能。
面对以上限制,麻省理工学院陈伟博士(现华中科技大学同济医学院基础医学院药理学系陈伟教授),基于博士后团队Robert Langer与Giovanni Traverso教授课题组的研究基础,并且受到刺头蠕虫附着于脊椎动物肠道中的带刺长鼻的启发,开发出一款动态全向粘附微针阵列系统(Dynamic Omnidirectional Adhesive Microneedle System, DOAMS)。此装置由感应局部胃环境触发的弹出装置和粘附于药片两端的DOAMS两部分组成,在感应到胃部低pH值环境后,弹出装置将粘附有DOAMS的药片弹出,在DOAMS的作用下药片将瞬时粘附于黏膜上,致使药片能长时间稳定地停留在特定部位,并诱导微孔道促进药物吸收,增大了口服片剂的生物利用度(图1)。该工作于2022年1月发表于Science子刊Science Advances(IF=14.136)期刊后,已下载5000余次。
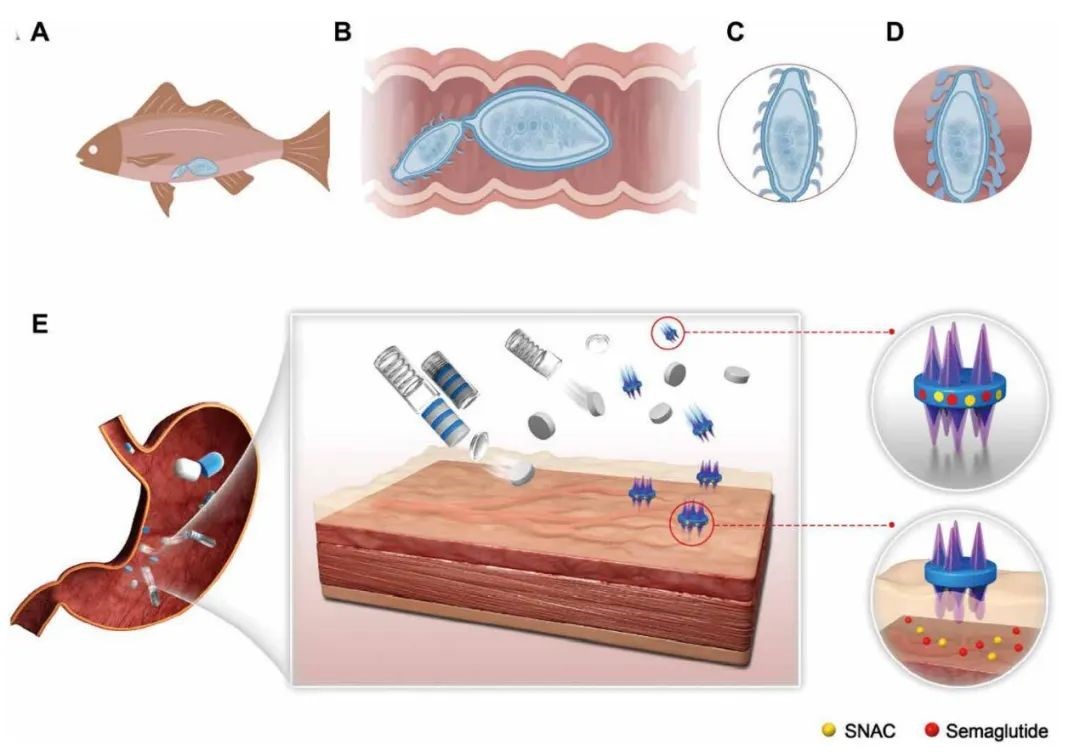
图1受刺头蠕虫启发的态全向粘附微针阵列系统的设计与作用方式。
研究团队在前期已经发展的智能血糖响应型微针贴片(Nat. Commun. 2017, 1777),自发富集病毒微针咽拭子(Matter 2020, 3 (5), 1589-1600),仿生定向牵引抗菌丝胶微针(Nano Lett. 2022, 22 (7), 2702-2711)以及可标记/易分离的仿生智能新冠疫苗微针贴片(ACS Nano 2022, 16 (5), 7512-7524)的基础上,构建了新型双层微针系统,内层结构提供机械强度,外层材料提供形变特性(图2)。口服后,药片上的微针接触胃组织表面,刺入粘膜层,会自发在粘膜组织内膨胀变形,产生互锁效应,提供一种不依赖于化学反应的生物粘附作用。除此之外,微针诱导产生的微孔道有助于索马鲁肽穿透消化道上皮组织,进入血液循环,从而表现出较高的吸收效率。